Ce înregistrează corpusculii neurotendinoși Golgi?
Întinderea puternică a tendonului.
Cristaloida este elastică sau fibroasă?
Unde este localizat stomacul ?
În loja gastrică, imediat sub diafragmă, în abdomen.
Care este forma fibrelor musculare cardiace?
Fibra musculară cardiacă este alungită, cilindrică şi ramificată.
Ce efecte poate avea inflamarea amigdalei faringiene?
• poate forma vegetații adenoide
• poate bloca trecerea aerului prin nazofaringe
Ce rol au ganglionii limfatici?
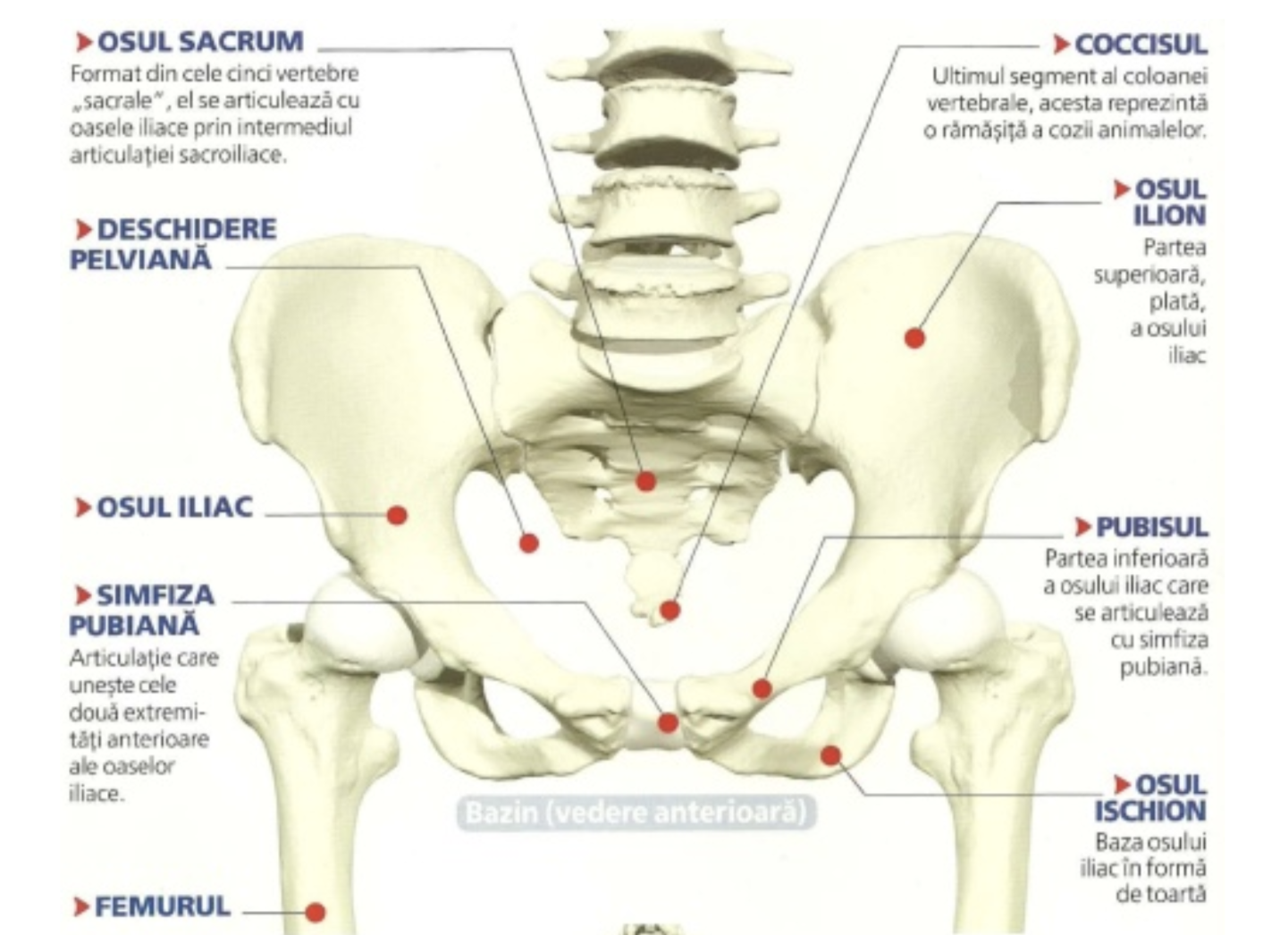
Osul coxal provine din sudarea a trei oase dinspre superior spre inferior:
Mușcăturile de artropode (țânțari, căpușe etc.)
Ce este abducția?
Abducția reprezintă îndepărtarea unui membru față de linia mediană a corpului
Ce bronhiole se continuă direct cu alveolele?
• bronhiolele respiratorii.
Care este principala arteră a circulației sistemice?
• aorta
Este afectat intelectul în modificările secreției STH?
leucemie cu monocite, tuberculoză, infecții fungice
aproximativ 7000/mm³
Stimulii cu frecvență crescută pot tetaniza inima?
Nu, inima nu poate fi tetanizată datorită inexcitabilității periodice, care împiedică sumarea contracțiilor.
Care sunt mediile refringente ale ochiului?
Ce tip de țesut formează sfincterul precapilar?
• mușchi circular
Gastrină și secretină
Crește depunerea calciului în oase și scade concentrația acestuia în sânge
Ce tip de substanță reprezintă coarnele medulare: cenușie sau albă?